Liposome hiện được coi là chất mang nano được sử dụng phổ biến nhất do tính tương thích sinh học cao. Liposome cũng được chứng minh là tăng cường khả năng hòa tan thuốc và phân phối có kiểm soát, cũng như khả năng sửa đổi bề mặt của chúng để giải phóng mục tiêu, kéo dài và bền vững.
1. Thành phần liposome
a. Lipid và phospholipid được sử dụng cho liposome
Về mặt cấu trúc, liposome là các túi hình cầu hoặc nhiều lớp hình cầu được tạo ra bằng cách tự lắp ráp các phospholipid chuỗi diacyl (lớp lipid kép) trong dung dịch. Màng phospholipid kép có một đuôi kỵ nước và một đầu ưa nước dẫn đến sự hình thành cấu trúc lưỡng tính. Liposome có thể được tạo ra từ cả phospholipid tự nhiên và tổng hợp. Thành phần lipid ảnh hưởng mạnh đến các đặc tính của liposome bao gồm: kích thước hạt, độ cứng, tính lưu động, tính ổn định và điện tích.
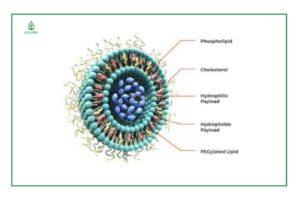
Ví dụ, liposome được điều chế từ phosphatidylcholine không bão hòa tự nhiên, như phosphatidylcholine trong trứng hoặc đậu tương, mang lại tính thẩm thấu cao và tính ổn định thấp. Mặc dù vậy, các liposome dựa trên phospholipid bão hòa như dipalmitoyl phosphatidylcholine dẫn đến cấu trúc lớp kép và gần như không thấm nước.
Nhóm ưa nước trong lipid có thể mang điện tích âm, điện tích dương hoặc điện tích zwitterionic (cả điện tích âm và điện tích dương trong cùng một phân tử). Điện tích của nhóm ưa nước cung cấp sự ổn định thông qua lực đẩy tĩnh điện. Nhóm lipid kỵ nước khác nhau về chiều dài chuỗi acyl, tính đối xứng và độ bão hòa. Các chất béo được sử dụng trong điều chế liposome có thể được phân loại là:
Lipid tự nhiên
Lớp màng kép của các tế bào bình thường chủ yếu là glycerophospholipids. Phospholipid bao gồm một đơn vị glycerol được liên kết với một nhóm phốt phát (PO4 2−) và với hai phân tử axit béo. Nhóm phốt phát cũng có thể được liên kết với phân tử hữu cơ nhỏ, chủ yếu hợp chất hữu cơ choline. Phospholipid tự nhiên có thể được lấy từ nhiều nguồn khác nhau như đậu nành, lòng đỏ trứng.
Phospholipid được phân loại là phosphatidylcholine (PC), phosphatidylethanolamine (PE), phosphatidylserine (PS), phosphatidylinositol (PI), phosphatidylglycerol (PG) và axit phosphatidic (PA) liên quan đến các nhóm đầu phân cực. Phospholipid tự nhiên kém ổn định hơn so với phospholipid tổng hợp trong quá trình điều chế liposome do đặc tính không bão hòa của chuỗi hydrocarbon.
Phospholipid tự nhiên bao gồm nhiều loại axit béo, một là axit béo no như axit palmitic (axit hexadecanoic, H3C-(CH2)14-COOH); axit margaric (axit heptadecanoic, H3C-(CH2)15-COOH) và loại còn lại là axit béo không no (axit oleic, hoặc axit 9Z-octadecenoic được xác định trong lecithin lòng đỏ trứng. Phospholipid và PC có nguồn gốc từ trứng được tạo thành từ các mẫu axit béo: axit palmitic (C16:0), axit stearic (C18:0), axit oleic (C18:1), axit linoleic (C18:2) và axit arachidonic (C20:4). Các axit béo này chiếm khoảng 92% tổng thành phần axit béo với sự hiện diện điển hình của axit béo không no C20:4 (n-6) và C22:6 (n-3) trong phospholipid của trứng. PC trứng chứa khoảng 40% 1-palmitoyl-2-oleoylphosphatidylcholine. Axit bão hòa chính là stearic trong PE và PS, và palmitic trong các chất béo khác.
Hơn nữa, mô hình axit béo có nguồn gốc đậu nành chiếm khoảng 95% axit palmitic (C16:0), axit stearic (C18:0), axit oleic (C18:1), axit linoleic (C18:2) và axit linolenic (C18:3). Vì các axit béo không no của PE, PS và PC chiếm hơn 50% tổng số axit nên chúng xuất hiện ở cả hai vị trí α- và β- của gốc glycerol của các phospholipid này.
Lipid tổng hợp
Phospholipid tổng hợp được tạo ra bằng cách biến đổi hóa học cụ thể đối với các vùng không phân cực và phân cực của phospholipid tự nhiên. Việc sửa đổi cho phép vô số loại phospholipid được xác định và phân loại rõ ràng. Các phospholipid tổng hợp bão hòa chính dựa trên việc sử dụng axit béo stearic và/hoặc palmitic. Ngoài ra, phospholipid tổng hợp có thể được tạo ra từ các axit béo hỗn hợp, axit béo không no trong cả hai hydrocacbon hoặc chỉ trong một chuỗi hydrocacbon.
b. Sterol
Steroid là lipid kỵ nước bao gồm cấu trúc bốn vòng. Sự đa dạng của steroid đến từ các nhóm chức năng khác nhau được gắn vào các vòng đó. Cholesterol là steroid chính thường được sử dụng trong điều chế liposome với tỷ lệ dưới 30% tổng số lipid để cải thiện độ cứng và ổn định của liposome vì nó được kết hợp trong lớp lipid kép của liposome.
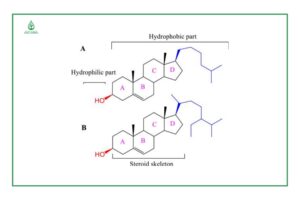
Trong một nghiên cứu so sánh về tác dụng của cholesterol và β-Sitosterol đối với các đặc tính của màng liposome, họ phát hiện ra rằng cả hai steroid đều làm giảm tính lưu động của màng liposome, tăng điện thế zeta tuyệt đối, gây ra những thay đổi đáng kể về kích thước hạt và giảm nhiệt độ chuyển pha DPPC (Tm) và entanpi.
c. Chất hoạt động bề mặt
Các chất hoạt động bề mặt được sử dụng trong các công thức liposome để thay đổi các đặc tính đóng gói và giải phóng của liposome thông qua việc giảm sức căng bề mặt giữa các pha không thể trộn lẫn vào nhau. Chất hoạt động bề mặt là các chất lưỡng tính chuỗi acyl đơn làm mất ổn định lớp lipid kép của các hạt nano liposome, do đó làm tăng khả năng biến dạng của túi nano.
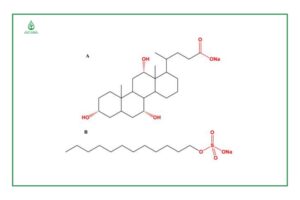
Các chất hoạt động bề mặt thường được sử dụng trong công thức liposome là: natri cholate, Span 60, Span 80, Tween 60 và Tween 80. Các liposome chứa chất hoạt động bề mặt khác nhau đã được sử dụng rộng rãi như một chất mang trong vận chuyển thuốc để tăng cường khả năng thẩm thấu qua da của các tác nhân trị liệu được bao bọc. Các liposome siêu biến dạng, còn được gọi là transfersome, là một hạt nano dựa trên chất hoạt động bề mặt với những phát hiện khả quan trong việc vận chuyển thuốc qua da.
Yếu tố then chốt làm cho liposome có thể biến dạng được là chất kích hoạt cạnh (chất hoạt động bề mặt). Chất kích hoạt cạnh có thể thay đổi lớp lipid kép của các túi làm tăng khả năng biến dạng của chúng. Các hạt nano này khác với các liposome thông thường ở chỗ chúng có thể phản ứng với áp suất thẩm thấu bằng cách biến đổi hình dạng nhanh chóng chỉ bằng năng lượng thấp. Hơn nữa, các liposome siêu biến dạng cho thấy sự gia tăng lưu lượng thuốc qua biểu bì khiến chúng trở thành phương tiện nano phù hợp hơn cho việc sử dụng thuốc hạ huyết áp tại chỗ.
2. Các loại liposome
Dựa trên thành phần và ứng dụng, liposome có thể được phân loại thành liposome thông thường, liposome tích điện, liposome ổn định tàng hình, liposome đích chủ động, liposome đáp ứng kích thích và liposome bong bóng.
a. Liposome thông thường
Những liposome này được tổng hợp từ phospholipid tự nhiên hoặc tổng hợp có hoặc không có cholesterol như là liposome thế hệ đầu tiên. Cholesterol được thêm vào để cải thiện tính lưu động của liposome, thay đổi độ cứng của lớp kép và độ ổn định của liposome. Wu và cộng sự tiết lộ rằng độ cứng của màng liposome giảm khi bổ sung cholesterol vào liposome bao gồm phospholipid đậu nành hydro hóa (HSPC) và DSPE-PEG2000.
Hơn nữa, liposome với một vài độ cứng cho thấy khả năng thâm nhập khối u và tăng cường hoạt động chống khối u. Do đó, cholesterol đóng một vai trò quan trọng đối với tính lỏng và độ cứng của lớp kép liposome, nhưng những đặc tính này bị ảnh hưởng bởi tỷ lệ mol cholesterol với các loại phospholipid được sử dụng cùng với bản chất của thuốc được bao bọc. Các liposome thông thường cho thấy thời gian lưu thông máu ngắn do dễ bị hệ thống thực bào đơn nhân loại bỏ với sự tích tụ nhanh chóng trong gan và lá lách.
Do đó, hệ thống thực bào đơn nhân cản trở việc phân phối các liposome thông thường đến vùng mục tiêu và hạn chế phân phối chúng đến các mô khác của cơ thể. Các liposome thông thường cũng cho thấy sự ổn định tương đối hạn chế trong in vitro. Vì vậy, liposome ổn định tàng hình đã được phát minh để tăng lưu thông máu và tăng cường sự ổn định của liposome in vivo.
b. Liposome tích điện
Axit oleic và N-[1(2,3-dioleoyloxy) propyl]-N,N,N-trimetylam-monium clorua (DOTAP) thường được sử dụng để điều chế liposome anion và cation tương ứng. Các liposome tích điện cho thấy độ ổn định của liposome cao hơn trong quá trình bảo quản, do các hạt tích điện đẩy nhau và giảm khả năng tổng hợp. Liposome cation được sử dụng trong liệu pháp gen do khả năng bao bọc thành công axit nucleic bằng lực hút tĩnh điện.
Các liposome cation thích hợp để cung cấp các đại phân tử tích điện âm khác nhau như DNA, RNA và oligonucleotide vì điện tích âm và kích thước khá lớn của chúng hạn chế sự khuếch tán thụ động của chúng vào tế bào. Các liposome cation cũng nhắm mục tiêu có chọn lọc các tế bào nội mô tạo mạch trong các khối u. Liposome cation được coi là một công cụ tiềm năng để cung cấp liệu pháp điều trị cho não.
Các liposome cation có thể đi qua BBB bằng chuyển mã qua trung gian thụ thể hoặc chuyển mã qua trung gian hấp thụ. Điện tích dương cao hơn trên bề mặt của liposome cation có thể ảnh hưởng đến quá trình lưu thông máu của chúng và dẫn đến tương tác tĩnh điện với các loại anion trong máu và làm tăng sự kết tụ của liposome làm giảm vị trí tác dụng của chúng. Gắn bề mặt của các liposome này bằng poly ethylene glycol (PEG) bảo vệ chúng khỏi các protein lưu thông, cải thiện hiệu quả của thuốc thông qua cải thiện thời gian tuần hoàn hệ thống và giảm khả năng sinh miễn dịch.
Các liposome anion ít ổn định hơn trong máu so với các liposome trung tính và cation; chúng cho thấy tỷ lệ thanh thải cao hơn. Các liposome anion thường được sử dụng để vận chuyển thuốc qua da vì chúng cải thiện các đặc tính thẩm thấu qua lớp sừng của da.
c. Liposome ổn định tàng hình
Các liposome thế hệ thứ hai này được đặc trưng bởi sự gắn bề mặt bằng các polyme tổng hợp, glycoprotein, polysacarit hoặc phối tử thụ thể đặc trưng để đạt được sự phân bố hẹp và tích lũy tại vị trí dự định. Axit huayluorinic, polyvinyl alcohol (PVA) và polyetylen glycol (PEG)) được coi là mô hình tốt nhất để bảo vệ không gian nguyên tử liposome. Liposome PEGylat là biểu hiện của liposome tàng hình. Các liposome ổn định tàng hình cho thấy thời gian lưu thông lâu hơn, dẫn đến tích lũy mục tiêu tốt hơn so với các thuốc liposome thông thường.
d. Liposome đích chủ động
Các liposome đích chủ động đại diện cho các liposome thế hệ thứ ba. Nhắm đích chủ động của liposome làm tăng tính chọn lọc của tương tác liposome với các tế bào bị bệnh và kích hoạt quá trình nội tiết qua trung gian thụ thể của liposome và tải trọng của nó vào mục tiêu tế bào mong muốn.
Nhiều chất mang nano liposome đã được phê duyệt để phân phối các tác nhân chống khối u theo cách thụ động dựa trên hiệu ứng tăng cường tính thấm và lưu giữ (EPR) của các tế bào ung thư. Nhắm mục tiêu thụ động không phân biệt giữa tế bào bình thường và tế bào bị bệnh; do đó, các liposome nhắm mục tiêu tế bào cụ thể đã được phát triển để tăng tích lũy và khu trú các chất chống khối u trong các tế bào bị bệnh. Khả năng nhắm đích của liposome có thể được tăng cường bằng cách kết hợp các gốc nhận dạng phân tử, điều này có thể dẫn đến việc vận chuyển thuốc với hiệu quả tốt hơn và tác dụng phụ thấp. Ví dụ, các chiến lược nhắm đích của liposome đã sử dụng các peptide đơn giản, protein (bao gồm cả kháng thể) hoặc các đoạn protein, carbohydrate, axit nucleic hoặc vitamin.
Cả liposome đích chủ động (liên hợp phối tử) và thụ động (‘không liên hợp’) đều được phân phối đến các tế bào đích thông qua cùng một cơ chế phân phối thụ động. Lĩnh vực liposome phối tử đích đã mở rộng nhanh chóng mặc dù một số liposome không nhắm mục tiêu đã tiếp cận phòng khám hoặc trong các thử nghiệm lâm sàng.
Những nỗ lực mới trong các hệ thống phân phối thuốc nhắm đích sử dụng axit béo không bão hòa đa, axit folic, axit hyaluronic hoặc oligopeptide làm gốc nhận dạng khối u. Các phối tử này gặp phải nhiều phạm vi thảo luận xung quanh ái lực và tính đặc hiệu của chúng mà không có cơ chế nhắm khối u đích chi tiết đi kèm với thành công hạn chế đối với một số phối tử nhỏ, bên cạnh sự phân hủy enzyme trong tuần hoàn hệ thống, khiến chúng không phù hợp với nhiều nghiên cứu in vivo. Gần đây, aptamer (một đoạn DNA, RNA hay peptide được chọn lọc nhân tạo ra để gắn với một phân tử đích nào đó) và các hạt nano chức năng aptamer có tính đặc hiệu và ái lực cao rất được chú ý trong các hệ thống phân phối thuốc theo đích.
Việc nhắm đích chủ động của các chất mang nano có thể đạt được thông qua liên hợp không cộng hóa trị hoặc cộng hóa trị của các phối tử đích với phân tử thuốc hoặc với bề mặt của chất mang nano để liên kết chọn lọc các dấu ấn sinh học đích biểu hiện quá mức trên các tế bào khối u. Sự kết hợp trực tiếp của thuốc với phối tử đích có thể phá vỡ sự nhận dạng của thụ thể/ phối tử và có thể làm thay đổi hiệu quả của thuốc.
Chất mang nano nhắm đích chủ động cho phép thuốc được khu trú trong vị trí tác dụng với hiệu quả cao hơn để giảm liều thuốc, giảm thiểu tác dụng phụ của thuốc và giảm sự thay đổi nồng độ thuốc trong máu. Các liposome tàng hình và thông thường thường cho thấy sự giải phóng chậm các loại thuốc được nạp và không hợp nhất với endosome (nội bào) sau khi nội hóa. Do đó, các liposome đáp ứng kích thích đã được giới thiệu để khắc phục những thách thức này.
e. Liposome đáp ứng kích thích
Các liposome đáp ứng kích thích là các hệ thống liposome thông minh thể hiện sự giải phóng nhanh chóng lượng thuốc của chúng khi có các kích thích hóa lý hoặc sinh hóa, như pH, nhiệt độ, thế oxy hóa khử, nồng độ enzyme, siêu âm, điện trường hoặc từ trường.
Các liposome đáp ứng kích thích nên chứa một thành phần nhất định kiểm soát tính ổn định và tính thấm của lớp lipid kép. Có hai loại cảm ứng cơ bản, từ xa và cục bộ. Cảm ứng từ xa đáp ứng với các kích thích bên ngoài bao gồm nhiệt, từ trường, ánh sáng, điện trường và siêu âm. Các chất kích hoạt cục bộ đáp ứng với các kích thích bên trong các mô đích, như pH, khả năng oxy hóa khử và enzyme.
f. Liposome bong bóng
Liposome bong bóng (liposome bọc khí) được kỳ vọng sẽ tạo ra những ứng dụng mới trong lĩnh vực chuyển gen và hệ thống phân phối thuốc. Gần đây, liposome đã được sử dụng để đóng gói khí hoạt tính sinh học và/hoặc thuốc để giải phóng thuốc được kiểm soát bằng siêu âm với khả năng tăng cường vận chuyển thuốc.
Các liposome bong bóng oxit nitric (NO) cung cấp một lựa chọn trị liệu NO tĩnh mạch khác biệt vượt qua các bong bóng siêu nhỏ thông thường, trong đó các liposome bảo vệ NO khỏi sự tìm kiếm của huyết sắc tố trong in vitro như thường xảy ra với NO tự do. Liposome bong bóng oxy (OBL) cho phép cố định giàu oxy với điều kiện pO2 cao của phổi. Điều này tách OBL khỏi các chất vận chuyển oxy dựa trên fluorocarbon và hemoglobin và duy trì việc sử dụng chúng như các giai đoạn hỗ trợ vận chuyển oxy.
Website: https://inrd.vn/
Fanpage: https://www.facebook.com/inrd2022









